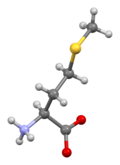
Métionin
 Rumus rangka bentuk kanonik métionin
| |||
| |||
| Wasta | |||
|---|---|---|---|
| Wasta IUPAC
Métionin
| |||
| Wasta lian
Asam 2-amino-4-(métiltio)butanoat
| |||
| Pananda | |||
Modél 3D (JSmol)
|
|||
| Abbreviations | Met, M | ||
| ChEBI |
| ||
| ChEMBL |
| ||
| ChemSpider | |||
| DrugBank |
| ||
| ECHA InfoCard | 100.000.393 | ||
| Nomer EC | 200-432-1 | ||
| KEGG |
| ||
PubChem CID
|
|||
| UNII |
| ||
CompTox Dashboard (EPA)
|
|||
| |||
| |||
| Sipat[2] | |||
| C5H11NO2S | |||
| Massa molar | 14921 g·mol−1 | ||
| Panampilan | White crystalline powder | ||
| Dénsitas | 1.340 g/cm3 | ||
| Titik lebur | 281 °C (538 °F; 554 K) decomposes | ||
| Soluble | |||
| Kaasaman (pKa) | 2.28 (carboxyl), 9.21 (amino)[1] | ||
| Farmakologi | |||
| V03AB26 (WHO) QA05BA90 (WHO), QG04BA90 (WHO) | |||
Iwal disebutkeun séjén, data nu dipidangkeun keur matéri dina kaayaan baku (dina 25 °C, 100 kPa). | |||
| Rujukan kotak info | |||
Métionin (lambangna Met atawa M)[3] (/mɪˈθaɪəniːn/)[4] nyaéta asam amino ésénsial pikeun manusa. Salaku prékursor asam amino sistéin jeung taurin, sanyawa multiguna sarupaning SAM-e, jeung antioksidan penting glutation, métionin mancén peran penting dina métabolisme jeung kaséhatan rupa-rupa spésiés.
Métionin ogé penting dina angiogenesis, tumuwuhna pembuluh getih. Supleméntasi métionin bisa natambaan anu karacunan tambaga.[5] Sabalikna, asupan métionin anu kaleuleuwihi, donor gugus métil dina métilasi DNA, tumali jeung tumuwuhna kangker dina sababaraha panalungtikan.[6][7] Métionin munggaran diisolasi taun 1921 ku John Howard Mueller.[8]
Watek biokimia
[édit | édit sumber]Métionin (lambangna Met atawa M; dikode ku kodon AUG) téh asam α-amino anu dipaké dina biosintésis protéin. Ieu ngandung gugus karboksil (dina wangun kurang proton −COO− dina kaayaan pH biologis), gugus amino (dina wangun leuwih proton −NH3+ dina kaayaan pH biologis) dina α-posisi ti gugus karboksil, sarta ranté gigir S-métil tioéter, kagolongkeun kana asam amino nonpolar alipatik.
Dina gén inti eukariot jeung Archaea, métionin nyandi pikeun kodon mitembeyan, hartina nandaan ngamimitian daérah koding jeung asam amino munggaran anu diproduksi dina polipéptida nalika translasi mRNA.[9]
Baca ogé
[édit | édit sumber]Rujukan
[édit | édit sumber]- ↑ Dawson, Rex M. C.; Elliott, Daphne C.; Elliott, William H.; Jones, K. M. (1959). Data for Biochemical Research. Oxford: Clarendon Press.
- ↑ Citakan:RubberBible62nd.
- ↑ "Nomenclature and Symbolism for Amino Acids and Peptides". IUPAC-IUB Joint Commission on Biochemical Nomenclature. 1983. Diarsipkan dari versi asli tanggal 9 October 2008. Diakses tanggal 5 March 2018. Archived 9 Oktober 2008 di Wayback Machine
- ↑ "Methionine". Oxford University Press. Archived 2018-01-27 di Wayback Machine
- ↑ "Methionine". WebMD.
- ↑ "A review of methionine dependency and the role of methionine restriction in cancer growth control and life-span extension". Cancer Treatment Reviews 38 (6): 726–36. 2012. doi:10.1016/j.ctrv.2012.01.004. PMID 22342103.
- ↑ "Methionine dependency and cancer treatment". Cancer Treatment Reviews 29 (6): 489–99. 2003. doi:10.1016/S0305-7372(03)00118-X. PMID 14585259.
- ↑ Pappenheimer AM (1987). "A Biographical Memoir of John Howard Mueller" (PDF). Washington D.C.: National Academy of Sciences.
- ↑ "Amino acids biosynthesis and nitrogen assimilation pathways: a great genomic deletion during eukaryotes evolution". BMC Genomics 12 Suppl 4: S2. December 2011. doi:10.1186/1471-2164-12-S4-S2. PMC 3287585. PMID 22369087. http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pmcentrez&artid=3287585.
Tutumbu kaluar
[édit | édit sumber]- Rudra, M. N.; Chowdhury, L. M. (30 September 1950). "Methionine Content of Cereals and Legumes". Nature 166 (568): 568. Bibcode 1950Natur.166..568R. doi:10.1038/166568a0. PMID 14780151.
- Webarchive template wayback links
- Chemical articles with multiple compound IDs
- Chemicals using indexlabels
- Chemical articles with multiple CAS registry numbers
- Chemical articles with multiple PubChem CIDs
- Chemical articles with multiple ChEBIs
- Articles without InChI source
- ECHA InfoCard ID ti Wikidata
- Articles containing unverified chemical infoboxes
- Chembox image size set
- Asam amino protéinogenik
- Asam amino glukogenik
- Asam amino sulpur
- Tioéter
- Asam amino ésénsial