Aldehida
Aldehida ngandung harti gugus fungsi nu diwangun ku hiji gugus karbonil terminal/tungtung, atawa hiji sanyawaan nu ngandung gugus karbonil terminal.
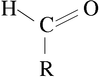
Struktur
[édit | édit sumber]Gugus fungsi aldehida nyaéta hiji gugus karbonil nu kabeungkeut kana hiji atom hidrogén jeung hiji atom karbon.
Karbon α & hidrogén α
[édit | édit sumber]Karbon α (alfa) hartina karbon nu meungkeut sacara langsung karbon na gugus karbonil, sedengkeun hidrogén α hartina atom hidrogén nu kabeungkeut ku karbon α.
Hidrogén α mibanda pKa 20.
Gugus karbonil
[édit | édit sumber]Molekul séjén nu ngandung gugus karbonil, nyaéta
Aldehida dingaranan ku tata ngaran IUPAC ku jalan ngaganti ahiran -a ku -al dina alkana indungna.
Pasipatan fisik
[édit | édit sumber]Gugus karbonil sipatna polar.
Kimia
[édit | édit sumber]Nyieun
[édit | édit sumber]Aya tilu métode utama pikeun nyieun aldehida:
- ngaréaksikeun alkohol primér jeung agén pangoksidasi,
- ngaréaksikeun alkana (mun aya hidrogén viinlatan) jeung ozon nu bakal ngabalukarkeun pegatna beungkeut C=C ngahasilkeun aldehida, dina prosés nu disebut ozonolisis.
- ngaréduksi éster ku DIBAL-H.
Cara utama sintésisna nyaéta ku oksidasi alkohol primér. Di laboratorium, ieu bisa kahontal ku cara manaskeun alkohol nu dicampur jeung réagen kromium (VI), leyuran asam kalium bikromat, nu diréduksi jadi Cr3+ héjo nalika rékasina. Bikromat leuwihna bakal ngoksidasi aldehida jadi asam karboksilat, so either the aldehyde is distilled out as it forms (if volatile), or milder methods such as PCC oxidation or Swern oxidation are used. The equation is shown below with propan-1-ol being oxidised to form propanal.
CH3CH2CH2OH —→ CH3CH2CHO
Prosés nu sarua dina réaksi nyieun péntanal tina péntan-1-ol digambarkeun di handap.
Réaksi umum
[édit | édit sumber]- aldehida + alkohol + asam atawau basa —→ hémiasetal
- hémiasetal + alkohol + katalis asam —→ asetal + cai
- Hémiasetal basajan biasana teu stabil, najan nu siklik kayaning glukosa mah aya. Asetal mah stabil, tapi mun lingkunganana asam bakal balik deui jadi aldehida.
- Nyampurkeun aldehida jeung agén pangoksidasi kayaning kalium permanganat, asam nitrat, atawa kromium (VI) oksida, bakal ngahasilkeun asam karboksilat.
- Nyampurkeun aldehida jeung réagen Tollens (nu dijieun ku cara ngeclakkeun natrium hidroksida kana leyuran pérak nitrat nu ngahasilkeun endapan pérak (I) oksida, lajeng nambahkeun leyuran amonia sacukupna pikeun ngaleyurkeun deui endapanana nepi ka ngahasilkeun kompléks [Ag(NH3)2]+) bakal malikkeun aldehida jadi asam karboksilat tanpa nyerang beungkeut ganda karbon-karbon. Tempo ogé oksidasi aldehida
- Aldehida bisa meta jeung cai (dina kaayaan asam atawa basa) ngahasilkeun hidrat, R-C(H)(OH)(OH), although these are only stable when strong electron withdrawing groups are present as in chloral hydrate. Mékanismena sarua jeung formasi hémiasetal.
- Aldehida bisa meta jeung HCN ngahasilkeun sianohidrin, R-C(H)(OH)(CN).
- Nyampurkeun aldehida jeung réagen Grignard bisa ngahasilkeun alkohol kalawan gugus nu diganti ti réagen Grignard.
- Nyampurkeun aldehida jeung hidrazin bakal ngaréduksi beungkeut C=O jadi CH2 via réaksi Wolff-Kishner.
- aldehida + nukléofil —→ sanyawa adisi karbonil tétrahédral
- aldehida + amonia atawa amina primér —→ sanyawa adisi karbonil tétrahédral
- sanyawa adisi karbonil tétrahédral + asam (katalis) —→ imina + cai
- aldehida + amonia atawa amina primér —→ sanyawa adisi karbonil tétrahédral
Kasatimbangan tautomér keto jeung énol dikatalisan ku asam.
Oksidasi & Réduksi
[édit | édit sumber]- Aldehida dioksidasi jadi asam karboksilat.
- Aldehida diréduksi jadi alkohol primér.
