Asam karboksilat
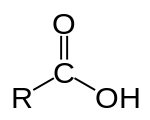


Dina kimia, asam karboksilat (ogé disebut asam alkanoat) nyaéta asam organik nu dicirikeun ku ayana gugus karboksil. Strukturna
R mangrupa hidrogén atawa gugus organik. Dina rumus kimia, ieu ogé biasa ditulis RCOOH).
Kaasaman, sebaran éléktron, jeung résonans
[édit | édit sumber]Asam karboksilat mangrupa asam lemah, sabab disosiasi molekul RCOOH ngan kira 1% nu jadi kation H+ jeung anion RCOO- na suhu rohangan dina leyuran cai.
Dua atom oxigén éléktronégatif cenderung metot éléktron ngajauhan hidrogén na gugus hidroxil, sedengkeun proton H+ sésana bisa leupas kalawan gampang. Muatan négatif sésana salajengna nyebar simétris di antara dua atom oxigén, sarta beungkeut karbon–oxigén mibanda ciri beungkeut ganda parsial (délokalisasi).
Ieu mangrupa hasil tina struktur résonans nu kaciptakeun ku ayana komponén karbonil na asam karboksilat, nu mun teu kitu gugus OH-na moal gampang kaleungitan H+-na (tempo alkohol).
Ayana gugus éléktronégatif (kayaning -OH atawa -Cl) nuturkeun gugus karboksilat bakal ngaronjatkeun kaasaman. antukna, pikeun conto, asam trikloroasétat (tilu gugus -Cl) mangrupa asam nu leuwih kuat batan asam laktat (hiji gugus -OH) nu leuwih kuat batan asam asetat (teu boga gugus séjén).
Réaksi
[édit | édit sumber]Asam karboksilat bisa dijieun ku jalan oksidasi lengkep alkohol primér.
Asam karboksilat meta jeung basa piekun ngahasilkeun uyah karboksilat, nalika hidrogén gugus -OH diganti ku ion logam. Asam étanoat (sarua jeung asam asetat) meta jeung natrium bikarbonat (baking soda) jadi natrium étanoat (natrium asetat), karbon dioxida, jeung cai:
- CH3COOH + NaHCO3 → CH3COONa + CO2 + H2O
Gugus karboxil ogé meta jeung gugus amina jadi beungkeut péptida sarta jeung alkohol jadi éster.
Asam karboksilat bisa diréduksi ku LiAlH4 jadi alkohol primér:
Contoh
[édit | édit sumber]Sababaraha asam karboksilat di antarana:
- HCOOH asam format (kapanggih dina panyeureud gegeremet, format nujul ka sireum)
- sadaya asam lemak, nu R-na mangrupa alkana dina asam jenuh atawa alkéna mun asamna teu jenuh
- CH3COOH asam asétat atawa asam étanoat (aya na cuka)
- CH3CH2COOH asam propanoat
- C6H5COOH asam bénzoat (natrium bénzoat, uyah natrium asam bénzoat dipaké salaku pangawét pangan)
- asam butirat
- CH2=CHCOOH asam akrilat
- asam laktat, aya na susu murni
- asam oksalat
- asam malonat
- asam suksinat
- asam glutarat
- asam adipat
- sadaya asam amino

